
Bài học rút ra chính
- Cơ quan Quản lý Thực phẩm và Dược phẩm (FDA) đã cấp phép sử dụng khẩn cấp (EUA) một phương pháp điều trị bằng kháng thể coronavirus do Eli Lilly thực hiện.
- Loại cocktail kháng thể được gọi là bamlanivimab và đã được phép sử dụng cho những bệnh nhân có nguy cơ cao, được chẩn đoán gần đây từ 12 tuổi trở lên.
- Eli Lilly cho biết họ có kế hoạch sản xuất tới một triệu liều bamlanivimab vào cuối năm 2020.
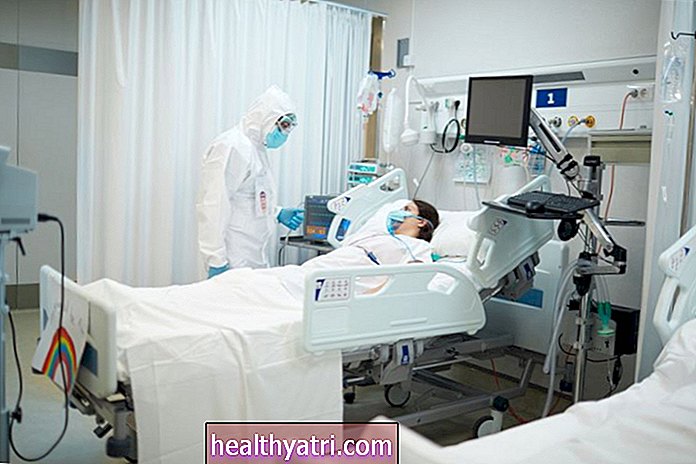
Cơ quan Quản lý Thực phẩm và Dược phẩm (FDA) đã thông báo trong một bức thư hôm thứ Hai rằng họ sẽ cấp giấy phép sử dụng khẩn cấp (EUA) đối với phương pháp điều trị bằng kháng thể trung hòa COVID-19 do công ty dược phẩm Eli Lilly thực hiện.
"Sự cho phép khẩn cấp này cho phép chúng tôi cung cấp phương pháp điều trị COVID-19 cho những bệnh nhân được chẩn đoán gần đây, có nguy cơ cao - thêm một công cụ có giá trị cho các bác sĩ chống lại gánh nặng ngày càng gia tăng của đại dịch toàn cầu này", Dave Ricks, Chủ tịch kiêm Giám đốc điều hành của Eli Lilly, cho biết trong một thông cáo báo chí.
Khả năng điều trị khả thi đến vào thời điểm COVID-19 lây nhiễm cho hơn 140.000 người mỗi ngày.
Phương pháp điều trị, được gọi là bamlanivimab (LY-CoV555), đã được phép điều trị COVID-19 từ nhẹ đến trung bình ở người lớn và trẻ em từ 12 tuổi trở lên với xét nghiệm COVID-19 dương tính và những người có nguy cơ cao tiến triển thành nặng COVID-19 và / hoặc nhập viện, theo tuyên bố của công ty. Cocktail kháng thể nên được sử dụng dưới dạng truyền tĩnh mạch duy nhất trong vòng 10 ngày kể từ khi phát triển các triệu chứng COVID-19.
“Như được minh họa bằng hành động hôm nay, FDA vẫn cam kết thúc đẩy sự phát triển và khả năng sẵn có của các phương pháp điều trị COVID-19 tiềm năng và cung cấp cho bệnh nhân bị bệnh quyền tiếp cận kịp thời với các liệu pháp mới nếu thích hợp, đồng thời hỗ trợ nghiên cứu để đánh giá thêm liệu chúng có an toàn hay không và hiệu quả, ”Ủy viên FDA Stephen M. Hahn, MD, cho biết trong một bản tin ngày 9 tháng 11. “Thông qua Chương trình Tăng tốc Điều trị Coronavirus của chúng tôi, FDA tiếp tục làm việc suốt ngày đêm và sử dụng mọi công cụ theo ý của chúng tôi cho những nỗ lực này.”
Tin tức của Eli Lilly được công bố vào cùng ngày Pfizer cho biết họ đã thu được kết quả ban đầu khả quan từ thử nghiệm vắc xin Pha 3 của mình. Nhưng Pfizer cho biết trong một tuyên bố rằng ngay cả với EUA đã được phê duyệt, họ sẽ không thể cung cấp số lượng lớn các liều thuốc có sẵn cho đến năm 2021.
Eli Lilly cho biết họ có kế hoạch sản xuất tới một triệu liều bamlanivimab vào cuối năm 2020.
Patrizia Cavazzoni, MD
"Sự cho phép khẩn cấp của FDA đối với bamlanivimab cung cấp cho các chuyên gia chăm sóc sức khỏe ở tuyến đầu của đại dịch này một công cụ tiềm năng khác để điều trị bệnh nhân COVID-19."
- Patrizia Cavazzoni, MDBamlanivimab là gì?
Tên có thể khó phát âm, nhưng mục đích của những kháng thể này rất đơn giản: “[Các] protein được tạo ra trong phòng thí nghiệm bắt chước khả năng của hệ thống miễn dịch để chống lại các kháng nguyên có hại như vi rút,” FDA cho biết trong thông cáo về bamlanivimab. Trong khi đó, bạn sẽ không gặp phải khó khăn gì.
Về cơ bản, bamlanivimab là một loại thuốc kháng thể nhắm vào protein COVID-19, cho phép nó ngăn chặn vi rút gắn và xâm nhập vào tế bào người.
“Sự cho phép khẩn cấp của FDA đối với bamlanivimab cung cấp cho các chuyên gia chăm sóc sức khỏe ở tuyến đầu của đại dịch này một công cụ tiềm năng khác để điều trị bệnh nhân COVID-19,” Patrizia Cavazzoni, MD, quyền giám đốc Trung tâm Nghiên cứu và Đánh giá Thuốc của FDA, cho biết trong FDA. giải phóng. “Chúng tôi sẽ tiếp tục đánh giá dữ liệu mới về tính an toàn và hiệu quả của bamlanivimab khi chúng có sẵn.”
Cả Bamlanivimab của Lilly và REGN-COV2 của Regeneron, loại cocktail kháng thể mà Tổng thống Trump nhận được khi ông được chẩn đoán mắc COVID-19, vẫn đang được xem xét. Tuy nhiên, REGN-COV2 vẫn chưa nhận được EUA từ FDA.
Sự khác biệt giữa EUA và Phê duyệt là gì?
EUA không có nghĩa là nhầm lẫn với sự chấp thuận của FDA.
“Khi xác định xem có ban hành EUA hay không, FDA đánh giá các bằng chứng sẵn có và cân bằng cẩn thận mọi rủi ro đã biết hoặc tiềm ẩn với mọi lợi ích đã biết hoặc tiềm năng của sản phẩm để sử dụng trong trường hợp khẩn cấp,” FDA cho biết trong tuyên bố của mình về bamlanivimab. “Dựa trên đánh giá của FDA về toàn bộ các bằng chứng khoa học có sẵn, cơ quan này xác định rằng có thể tin rằng bamlanivimab có thể có hiệu quả trong việc điều trị những bệnh nhân không nhập viện với COVID-19 ở mức độ nhẹ hoặc trung bình”.
Trong trường hợp của EUA, “những lợi ích đã biết và tiềm năng lớn hơn những rủi ro đã biết và tiềm ẩn đối với thuốc”.
Cái gì tiếp theo?
Chính phủ Hoa Kỳ đã mua 300.000 liều bamlanivimab, theo bản tin của Eli Lilly, sẽ miễn phí cho người Mỹ (ngoại trừ các cơ sở y tế có thể tính phí sử dụng thuốc).







-for-hip-replacement.jpg)




.jpg)








.jpg)

