những hình ảnh đẹp
Bài học rút ra chính
- Cơ quan Quản lý Thực phẩm và Dược phẩm (FDA) sẽ yêu cầu các nhà sản xuất vắc-xin cung cấp hai tháng dữ liệu an toàn trước khi phê duyệt vắc-xin COVID-19 cho công chúng sử dụng.
- FDA tin rằng khoảng thời gian hai tháng sẽ cho phép đủ thời gian để các tác dụng phụ có thể xảy ra hoặc kết quả bất lợi của vắc-xin tiềm năng xuất hiện.
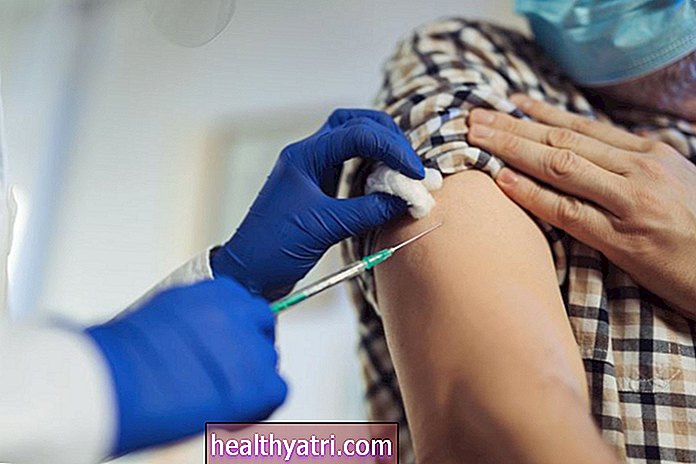
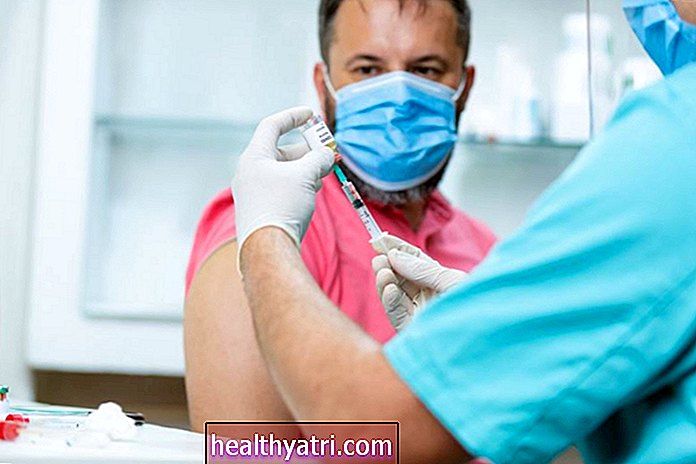
Vào ngày 6 tháng 10, Cơ quan Quản lý Thực phẩm và Dược phẩm (FDA) thông báo rằng họ sẽ yêu cầu các nhà sản xuất vắc-xin COVID-19 chia sẻ dữ liệu an toàn trong hai tháng trước khi cơ quan này phê duyệt vắc-xin cho công chúng sử dụng. công chúng ngày càng mất lòng tin về tính an toàn của vắc xin COVID trong tương lai.
Thuốc chủng ngừa COVID-19: Cập nhật loại vắc-xin nào có sẵn, ai có thể tiêm và mức độ an toàn của chúng.
Yêu cầu mới của FDA
Theo yêu cầu mới của FDA, sẽ cần có hai tháng dữ liệu theo dõi về sức khỏe của những người tình nguyện thử nghiệm lâm sàng sau khi họ nhận được liều vắc-xin thứ hai. FDA có thể chọn cấp phép sử dụng khẩn cấp cho nhà sản xuất vắc-xin. —Một chỉ định cho phép sử dụng công khai một sản phẩm — nếu các yêu cầu mới được đáp ứng.
Shobha Swaminathan, MD
An toàn là điều cốt lõi để đảm bảo rằng mọi người tin tưởng vào công việc mà chúng tôi đang làm.
- Shobha Swaminathan, MDFDA giải thích trong hướng dẫn của mình rằng họ muốn xem dữ liệu từ các thử nghiệm Giai đoạn 3 khi những người tham gia đã hoàn thành phác đồ vắc xin đầy đủ và trong hai tháng sau đó. FDA tin rằng mốc thời gian này sẽ cung cấp "thông tin đầy đủ để đánh giá hồ sơ rủi ro lợi ích của vắc xin."
Theo hướng dẫn, FDA sẽ xem xét "các sự kiện bất lợi; các trường hợp mắc bệnh COVID-19 nghiêm trọng giữa các đối tượng nghiên cứu; và các trường hợp COVID-19 xảy ra trong khung thời gian khi đáp ứng miễn dịch thích nghi (thay vì bẩm sinh) và trí nhớ với vắc xin sẽ chịu trách nhiệm về hiệu ứng bảo vệ. "
FDA cũng nói rằng cần phải có đủ “trường hợp COVID-19 nghiêm trọng trong số các đối tượng nghiên cứu” để chứng minh rằng có ít nguy cơ người mắc các biến chứng nghiêm trọng do vắc-xin.
Ngoài ra, FDA mong đợi các nhà sản xuất chứng minh dữ liệu liên quan đến một số hội chứng — cụ thể là bệnh hô hấp tăng cường liên quan đến vắc-xin (ERD) từ vắc-xin. “Tổng cộng năm trường hợp COVID-19 nghiêm trọng trở lên trong nhóm giả dược nói chung sẽ là đủ để đánh giá xem liệu sự phân chia trường hợp COVID-19 nghiêm trọng giữa nhóm vắc xin và nhóm giả dược hỗ trợ một hồ sơ nguy cơ lợi ích thuận lợi hay ngược lại làm tăng mối quan tâm. "
Hiện có 11 loại vắc-xin đang trong giai đoạn 3 (giai đoạn cuối) của thử nghiệm lâm sàng. Tuy nhiên, một số thử nghiệm do một số công ty dược phẩm lớn thực hiện gần đây đã bị tạm dừng sau khi ít nhất một người tham gia nghiên cứu mắc bệnh nghiêm trọng không rõ nguyên nhân.
Trường hợp chờ 2 tháng
“Tôi nghĩ thật tuyệt khi FDA đang yêu cầu chúng tôi có dữ liệu an toàn trong hai tháng”, chuyên gia về bệnh truyền nhiễm Shobha Swaminathan, MD, một phó giáo sư và điều tra viên chính cho thử nghiệm vắc xin Moderna COVID-19 tại Trường Y Rutgers New Jersey. Trung tâm Nghiên cứu Lâm sàng nói với Verywell. “An toàn là điều cốt lõi quan trọng trong việc đảm bảo rằng mọi người tin tưởng vào công việc mà chúng tôi đang làm”.
Swaminathan giải thích rằng các tác dụng phụ phổ biến nhất từ vắc-xin xảy ra trong khoảng thời gian hai tháng. “Hầu hết các phản ứng phụ của vắc-xin, chẳng hạn như sốt, mệt mỏi và phản ứng tại chỗ tiêm xảy ra trong tuần đầu tiên, và những phản ứng phức tạp hơn có thể xảy ra trong sáu tuần. Đó là lý do tại sao tối thiểu hai tháng là hữu ích để phát hiện những gì có thể đang xảy ra. "
Shobha Swaminathan, MD
Đừng vội kết luận về quy trình khoa học. Có rất nhiều thông tin sai lệch ngoài đó.
- Shobha Swaminathan, MDSwaminathan nói rằng khung thời gian là “cố gắng cân bằng nhu cầu công cộng mà không ảnh hưởng đến an toàn.” Cô hy vọng rằng hướng dẫn của FDA sẽ giúp thay đổi nhận thức của công chúng về quy trình phát triển vắc xin.
Swaminathan cho biết: “Công chúng có quan niệm rằng việc nghiên cứu vắc-xin COVID-19 đang được gấp rút trước kế hoạch và một số người lo lắng rằng nó sẽ phải trả giá bằng các biện pháp an toàn, điều này thực sự không đúng. sẽ đưa ra quyết định nếu thông tin an toàn mà họ có [từ các nhà nghiên cứu] là đầy đủ. ”
Nhìn chung, Swaminathan kêu gọi mọi người tin tưởng vào quá trình này. “Đừng vội kết luận về quy trình khoa học. Có rất nhiều thông tin sai lệch ngoài đó. "
Điều này có ý nghĩa gì đối với bạn
Yêu cầu của FDA về dữ liệu theo dõi trong hai tháng sau khi mọi người nhận được vắc-xin COVID-19 sẽ giúp đảm bảo rằng bất kỳ tác dụng phụ tiềm ẩn nào được phát hiện trước khi vắc-xin được cung cấp cho công chúng. Tuy nhiên, quá trình này cuối cùng có thể mất nhiều thời gian hơn.
Công chúng nên tin tưởng rằng quy trình phát triển và phê duyệt vắc-xin là an toàn và FDA sẽ không phê duyệt vắc-xin cho đến khi vắc-xin sẵn sàng — và an toàn.