Trong khi một số nhà sản xuất vắc-xin đang sử dụng các phương pháp tiếp cận mới để chống lại bệnh do coronavirus 2019 (COVID-19), những nhà sản xuất khác đang chuyển sang các phương pháp được thiết lập hơn để chấm dứt đại dịch.
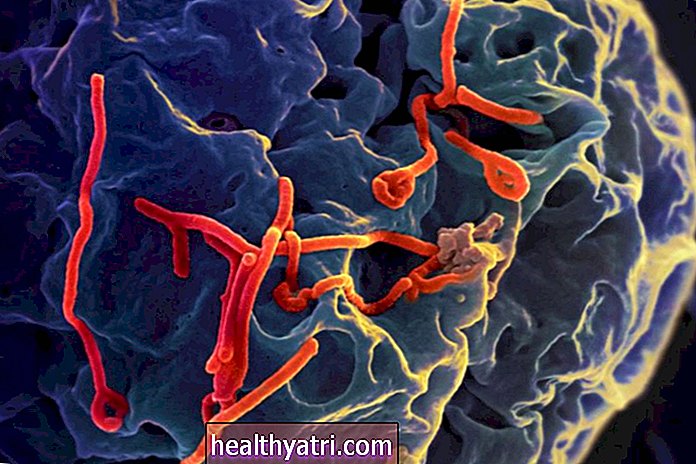
AstraZeneca và Đại học Oxford đã nghiên cứu một loại vắc xin dựa trên adenovirus, ChAdOx1 nCoV-19 (AZD1222). Thuốc chủng này là một loại vắc-xin vectơ vi-rút sử dụng một loại vi-rút adenovirus đã được sửa đổi — loại vi-rút gây ra cảm lạnh thông thường — có chứa vật chất di truyền từ vi-rút SARS-CoV-2. Vắc xin đã được phát triển một cách nhanh chóng vì công nghệ vắc xin này đã có từ nhiều thập kỷ trước.
Oxford đã nghiên cứu vắc xin dựa trên adenovirus cho một số bệnh khác như virus Zika khi COVID-19 xuất hiện. Các nhà nghiên cứu đã điều chỉnh một adenovirus của tinh tinh suy yếu để phát triển vắc-xin và giai đoạn 1 thử nghiệm bắt đầu vào tháng 4 năm 2020, với hơn 1.000 vắc-xin được tiêm ở Vương quốc Anh.
Kết quả thử nghiệm giai đoạn 3 ban đầu đã được công bố vào đầu tháng 12 và điều tra mức độ hoạt động của vắc-xin ở hơn 11.000 trong số gần 24.000 người trên 18 tuổi đăng ký tham gia vào bốn nhóm thử nghiệm ở Vương quốc Anh, Brazil và Nam Phi.
Đã có một số tranh cãi xung quanh loại vắc xin này, với sự khác biệt về liều lượng trong một số nhóm nghiên cứu và việc Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) yêu cầu tạm dừng thử nghiệm ở Hoa Kỳ vì bệnh tật không rõ nguyên nhân. FDA đã khởi động lại thử nghiệm sau khi xem xét dữ liệu an toàn.
Chưa có bất kỳ phiên điều trần nào được lên lịch theo giấy phép sử dụng khẩn cấp của FDA và cuộc thử nghiệm lâm sàng của Hoa Kỳ dự kiến kéo dài đến tháng 9 năm 2021.
Hình ảnh zoranm / GettyLàm thế nào nó hoạt động
Vắc xin AstraZeneca-Oxford là vắc xin vectơ siêu vi khuẩn adenoviral tái tổ hợp. Vắc xin tái tổ hợp sử dụng một phần nhỏ vật liệu di truyền từ mầm bệnh, như SARS-CoV-2, để kích hoạt phản ứng miễn dịch. Một phần cụ thể của vi-rút có thể được nhắm mục tiêu và vắc-xin tái tổ hợp thường an toàn để sử dụng cho nhiều người — ngay cả những người có vấn đề sức khỏe mãn tính hoặc những người bị suy giảm miễn dịch.
Vắc xin AstraZeneca-Oxford là vắc xin adenovirus tái tổ hợp sử dụng mầm bệnh sống đã được làm yếu. Một nhược điểm của vắc-xin vectơ vi-rút tuyến trùng tái tổ hợp là các mũi tiêm nhắc lại có thể được yêu cầu theo thời gian. Ví dụ về các loại vắc-xin tái tổ hợp tương tự (không sử dụng mầm bệnh sống) là vắc-xin phế cầu và vắc-xin phòng bệnh não mô cầu. Mặc dù vắc-xin tái tổ hợp phổ biến, vắc-xin dựa trên adenovirus duy nhất được bán trên thị trường thuộc loại này là vắc-xin phòng bệnh dại cho động vật.
Vắc xin adenovirus có thể gây ra một số vấn đề trong đó adenovirus phổ biến đến mức vắc xin có thể không hiệu quả sau khi tiêm liều tăng cường hoặc một số người có thể đã có miễn dịch với vi rút được sử dụng trong vắc xin.
Vắc xin AstraZeneca-Oxford đã được thử nghiệm bằng cách sử dụng hai liều tiêm cách nhau khoảng một tháng. Liều lượng được sử dụng trong các thử nghiệm không rõ ràng - với các tài khoản khác nhau về những thay đổi liều lượng được dịch vụ tin tức Reuters tiết lộ lần đầu tiên. Các phóng viên của hãng thông tấn này đã được AstraZeneca và Oxford đưa ra hai câu trả lời khác nhau về việc liệu một nhóm nhỏ trong nhóm nghiên cứu của Vương quốc Anh đã nhận được một nửa liều vắc xin có mục đích hay tình cờ. Sự khác biệt đã được phát hiện sau khi kết quả sơ bộ được công bố.
Làm thế nào hiệu quả là nó?
Cho dù là tình cờ hay cố ý, việc thay đổi liều lượng dường như là một điều may mắn. Theo báo cáo thử nghiệm, vắc xin AstraZeneca-Oxford trung bình có hiệu quả khoảng 70%. Tuy nhiên, mức trung bình này được tính toán sau khi quan sát thấy tỷ lệ hiệu quả 62% ở những người nhận đủ liều vắc xin so với 90% hiệu quả ở những người đã tiêm nửa liều. một nửa liều vắc xin có thể hoạt động tốt hơn liều đầy đủ thứ hai.
Khi nào nó sẽ sẵn sàng?
Nếu và khi nào vắc-xin sẽ có sẵn là một câu hỏi lớn. AstraZeneca đã chuẩn bị thông tin phân phối khi kết quả sơ bộ được công bố, nhưng những tranh cãi về việc liệu việc sử dụng một nửa liều vắc-xin có cố ý hay không và việc tạm dừng thử nghiệm vì lo ngại về tính an toàn có thể đã làm chậm tiến độ của vắc-xin. Công ty cho biết các thử nghiệm vẫn đang được tiến hành trên khắp thế giới, nhưng điều đó - đang chờ sự chấp thuận của cơ quan quản lý - có thể có tới 3 tỷ liều vào năm 2021. Một số quốc gia đã đặt hàng liều vắc-xin và cho phép sử dụng trong trường hợp khẩn cấp.
Sau khi có sẵn, vắc-xin có thể được phân phối dễ dàng hơn so với một số lựa chọn khác. Thay vì nhiệt độ quá lạnh như một số lựa chọn vắc-xin khác, vắc-xin AstraZeneca-Oxford sẽ chỉ yêu cầu làm lạnh tiêu chuẩn và ước tính có giá khoảng $ 3 đến $ 4 cho mỗi liều.
Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh (CDC) đang dẫn đầu các nỗ lực tiêm chủng và tất cả các đơn đặt hàng vắc xin COVID-19, bất kể nhà sản xuất nào, đều sẽ thông qua cơ quan này. CDC cũng đang giám sát việc phân phối vắc xin. Ủy ban Cố vấn của CDC về Thực hành Tiêm chủng (ACIP) đã đưa ra các khuyến nghị về cách ưu tiên nguồn cung cấp vắc xin. Nhân viên y tế và những người sống trong các cơ sở chăm sóc dài hạn là những nhóm ưu tiên đầu tiên nhận vắc xin COVID-19 được phép.
Theo CDC, có hơn 18 triệu nhân viên y tế ở Hoa Kỳ và khoảng 1,3 triệu người Mỹ sống trong các cơ sở chăm sóc dài hạn. Mỗi người trong số những người này sẽ cần được tiêm hai liều vắc-xin cho phép cho đến nay. . CDC ước tính rằng sẽ mất vài tháng trước khi nguồn cung vắc xin bắt kịp nhu cầu. Hướng dẫn về ai sẽ nhận vắc-xin và thời điểm sẽ được quyết định khi nguồn cung cấp có sẵn. Chỉ riêng Hoa Kỳ có dân số khoảng 330 triệu người - có nghĩa là gần 700 triệu liều vắc-xin sẽ cần thiết để tiêm chủng cho toàn nước Mỹ nếu các vắc-xin khác theo liều hai vắc-xin.
Các sở y tế của tiểu bang và địa phương đang phối hợp nỗ lực để phân phối liều lượng vắc xin khi chúng có sẵn. Thuốc chủng ngừa phải có sẵn ở cả văn phòng bác sĩ và các địa điểm bán lẻ như hiệu thuốc cung cấp các loại vắc-xin khác.
Thuốc chủng ngừa COVID-19: Cập nhật loại vắc-xin nào có sẵn, ai có thể tiêm và mức độ an toàn của chúng.
Ai Có thể Nhận Thuốc chủng ngừa AstraZeneca?
Thử nghiệm lâm sàng ban đầu cho vắc-xin AstraZeneca-Oxford tập trung vào những người từ 18 đến 55 tuổi và các thử nghiệm mới với những người trên 55 tuổi đã bắt đầu vào tháng Tám. Đã có những thử nghiệm liên quan đến trẻ em, nhưng nhóm đó đã bị xóa khỏi dữ liệu thử nghiệm vào giữa tháng 12. AstraZeneca và Oxford chưa đưa ra bất kỳ tuyên bố nào về sự thay đổi này.
Tác dụng phụ và các sự kiện bất lợi
Nói chung, các tác dụng phụ của vắc-xin COVID-19 bao gồm đau cánh tay, sưng và đỏ ở nơi tiêm vắc-xin. Tuy nhiên, đã có một số tác dụng phụ khác được báo cáo, bao gồm cả tác dụng dẫn đến việc tạm dừng thử nghiệm lâm sàng.
Phản ứng có hại được coi là phản ứng của thuốc do vắc-xin trực tiếp gây ra, trong khi tác dụng phụ là phản ứng vật lý đối với thuốc. Báo cáo sơ bộ về vắc xin được công bố trênĐầu ngóncho thấy kết quả nói chung tốt về tác dụng phụ, nhưng có một số phản ứng phụ liên quan đến.
Có ba trường hợp bị viêm tủy cắt ngang - một tình trạng có viêm tủy sống - ở những người đã được chủng ngừa.Theo báo cáo thử nghiệm, những căn bệnh này được xác định là không thể do vắc-xin gây ra. Một số trường hợp tử vong cũng được báo cáo trong nghiên cứu (hầu hết ở nhóm chứng), nhưng những trường hợp tử vong đó không liên quan đến vắc-xin và là do các sự cố như tai nạn giao thông và giết người.
Tài trợ và Phát triển
Vắc xin được phát triển thông qua sự hợp tác giữa Oxford và AstraZeneca. Hỗ trợ kinh phí cho nghiên cứu cũng được cung cấp bởi Nghiên cứu và Đổi mới Vương quốc Anh, Quỹ Bill & Melinda Gates, Trung tâm Nghiên cứu Y sinh NIHR Oxford, và Thung lũng Thames và Mạng lưới Nghiên cứu Lâm sàng NIHR của Nam Midland.