wera Rodsawang / Hình ảnh Getty
Bài học rút ra chính
- Một loại vắc xin RNA thông tin (mRNA) mới đã trở thành loại vắc xin COVID-19 đầu tiên được phép sử dụng khẩn cấp ở Hoa Kỳ
- Các nhà nghiên cứu đang nghiên cứu 10 mẫu vắc xin hiện có khác nhau để tạo ra vắc xin COVID-19
- Vắc xin cần phải có hiệu quả ít nhất 70% để loại trừ COVID-19
- Theo dõi nhanh vắc xin có nghĩa là bỏ qua các biện pháp bảo vệ
Cuộc chạy đua tìm kiếm vắc xin an toàn và hiệu quả cho COVID-19 (bệnh do coronavirus 2019) là chưa có tiền lệ trong lịch sử y học hiện đại. Không phải kể từ đại dịch AIDS nếu những năm 1980 và 90 có các nhà khoa học, chính phủ và doanh nghiệp cùng nhau nỗ lực phối hợp để chia sẻ kiến thức và nguồn lực mà một ngày nào đó có thể dẫn đến việc phát triển một loại vắc-xin bảo vệ hoàn toàn.
Cũng như đại dịch AIDS, có rất nhiều điều mà các nhà khoa học phải tìm hiểu về loại virus này.
Nhưng có hy vọng. Tính đến tháng 12 năm 2020, có không dưới 233 ứng viên vắc xin đang được phát triển tích cực ở Bắc Mỹ, Châu Âu và Châu Á, với mục tiêu đưa ít nhất một vắc xin hoàn chỉnh ra thị trường vào năm 2021.
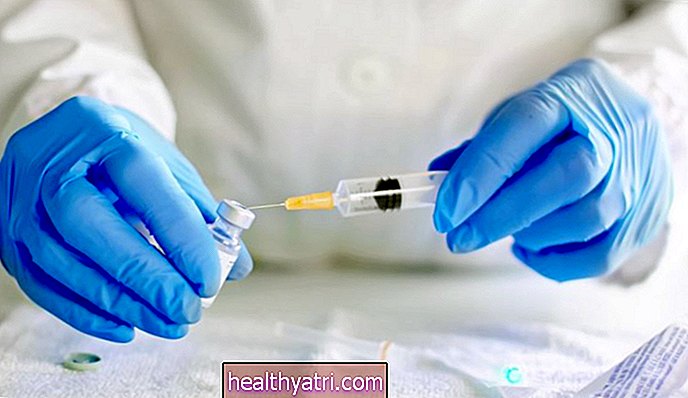
Vào ngày 11 tháng 12, Cục Quản lý Thực phẩm và Dược phẩm (FDA) đã cấp phép sử dụng khẩn cấp cho một ứng cử viên vắc xin COVID-19 do Pfizer và BioNTech đồng phát triển. Việc sử dụng khẩn cấp này được chấp thuận cho những người từ 16 tuổi trở lên. Một ứng cử viên vắc-xin COVID-19 khác từ Moderna đã được cấp phép sử dụng khẩn cấp vào ngày 18 tháng 12. Cả hai vắc-xin đều là vắc-xin RNA thông tin mới (mRNA) mang các chỉ dẫn di truyền cho các tế bào miễn dịch của chúng ta để tạo ra một phần của protein kích hoạt phản ứng miễn dịch với COVID -19.
Tại sao điều này lại quan trọng
Dù có vẻ khó khăn như những thách thức, vắc-xin vẫn là cách hiệu quả nhất để ngăn chặn tình trạng đóng cửa toàn cầu và các biện pháp làm xa rời xã hội đã xác định đại dịch COVID-19 ban đầu.
Mục tiêu và thách thức
Dòng thời gian tự nó đặt ra những thách thức to lớn. Cho rằng vắc xin mất trung bình 10,71 năm để phát triển từ khi bắt đầu nghiên cứu tiền lâm sàng cho đến khi phê duyệt quy định cuối cùng, các nhà khoa học được giao nhiệm vụ nén dòng thời gian theo cách mà hầu như chưa từng có trong nghiên cứu vắc xin.
Để vắc-xin được coi là khả thi, vắc-xin cần phải an toàn, rẻ tiền, ổn định, dễ sản xuất trên quy mô sản xuất và dễ dàng sử dụng cho càng nhiều người trong số 7,8 tỷ người sống trên hành tinh này.
Đồng thời, nếu một loại vắc xin để chấm dứt đại dịch, nó sẽ cần phải có hiệu lực cao, thậm chí cao hơn vắc xin cúm. Bất cứ điều gì thiếu hụt này có thể làm giảm sự lây lan của các bệnh nhiễm trùng, nhưng không thể ngăn chặn chúng.
Chỉ 6% vắc xin đang được phát triển được thực hiện từ nghiên cứu tiền lâm sàng đến khi tung ra thị trường.
Hiệu quả của vắc xin
Theo Tổ chức Y tế Thế giới (WHO), để vắc-xin loại trừ hoàn toàn COVID-19, vắc-xin cần phải có hiệu quả không dưới 70% trên cơ sở dân số và bảo vệ bền vững trong ít nhất một năm. Ở cấp độ này, vi rút sẽ ít có khả năng đột biến hơn khi nó truyền từ người sang người và có nhiều khả năng tạo ra khả năng miễn dịch theo bầy đàn (trong đó phần lớn quần thể phát triển khả năng kháng miễn dịch đối với vi rút).
Những điểm chuẩn này là vô cùng tham vọng, nhưng không phải là không thể.
Với hiệu quả 60%, WHO cho rằng các đợt bùng phát sẽ vẫn xảy ra và khả năng miễn dịch của bầy đàn sẽ không được xây dựng đủ mạnh để chấm dứt đại dịch.
Vắc xin COVID-19 với 50% hiệu quả, trong khi có lợi cho những người có nguy cơ cao, sẽ không ngăn ngừa bùng phát cũng như không làm giảm căng thẳng cho các hệ thống chăm sóc sức khỏe tuyến đầu nếu bùng phát.
Ví dụ, hiệu quả của vắc xin cúm là dưới 45% trong mùa cúm 2019-2020, theo Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh (CDC). Một số thành phần vắc-xin riêng lẻ chỉ có hiệu quả 37%.
Thuốc chủng ngừa mRNA cho COVID-19
Pfizer đã công bố vào ngày 18 tháng 11 rằng thử nghiệm vắc xin giai đoạn III của họ đã chứng minh 95% hiệu quả chống lại COVID-19. Moderna đã công bố vào ngày 30 tháng 11 rằng thử nghiệm vắc xin giai đoạn III của nó cho thấy 94% hiệu quả chống lại COVID-19 nói chung và cũng 100% hiệu quả chống lại bệnh nặng . Đánh giá ngang hàng vẫn đang chờ xử lý cho các thử nghiệm này.
Các cơ quan y tế có thể phê duyệt một loại vắc xin có hiệu lực kém hơn tối ưu nếu lợi ích (đặc biệt đối với người già và người nghèo) lớn hơn nguy cơ.
Giá cả
Một loại vắc-xin không thể được coi là khả thi nếu nó không phải là giá cả phải chăng.
Không giống như vắc-xin cúm, được sản xuất hàng loạt bằng cách tiêm vi-rút vào trứng gà, cả COVID-19 và bất kỳ anh em họ coronavirus nào của nó (như SARS và MERS) đều không thể tái tạo trong trứng. Do đó, cần phải có một công nghệ sản xuất hoàn toàn mới để phù hợp với khối lượng sản xuất vắc xin cúm hàng năm, trong đó hơn 190 triệu liều được cung cấp ở Hoa Kỳ mỗi năm.
Các vắc xin di truyền mới, bao gồm các ứng cử viên vắc xin Pfizer-BioNTech và Moderna, được phát triển trong các ống nghiệm hoặc bể chứa. Chúng không cần phải được nuôi trong trứng hoặc tế bào, điều này giúp tiết kiệm thời gian và chi phí trong quá trình phát triển. Mặc dù, đây là lần đầu tiên chúng được sản xuất hàng loạt nên vẫn chưa biết hết chi phí và nhiều khâu hậu cần.
Hoa Kỳ có hợp đồng mua liều lượng vắc xin mRNA từ Pfizer-BioNTech và Moderna, nhưng chi phí và khả năng tiếp cận của các loại vắc xin này và các loại vắc xin khác ở nhiều quốc gia trên thế giới vẫn chưa được xác định.
Chính phủ Hoa Kỳ có hợp đồng với Pfizer và BioNTech cho đơn đặt hàng ban đầu là 100 triệu liều với giá 1,95 tỷ đô la và có quyền mua tới 500 triệu liều bổ sung. Những người nhận vắc xin được tiêm miễn phí. Vắc xin cũng đã được cấp phép sử dụng khẩn cấp ở Anh, Bahrain, Ả Rập Xê Út, Canada và Mexico.
Chính phủ liên bang có hợp đồng trị giá 1,5 tỷ đô la với Moderna cho 100 triệu liều vắc-xin và tùy chọn mua thêm 400 triệu liều (Chính phủ đã yêu cầu thêm 100 triệu). Nó cũng giúp tài trợ cho sự phát triển của mình với một hợp đồng trị giá 955 triệu đô la, nâng tổng số tiền ban đầu lên 2,48 tỷ đô la. Nếu nó nhận được ủy quyền khẩn cấp, nó cũng sẽ được trao miễn phí cho những người ở Hoa Kỳ.
Phân phối
Sau khi vắc xin COVID-19 được phát triển, thách thức tiếp theo là phân phối chúng một cách công bằng, đặc biệt nếu năng lực sản xuất bị hạn chế. Điều này đòi hỏi nghiên cứu dịch tễ học rộng rãi để xác định quần thể nào có nguy cơ bị bệnh và tử vong cao nhất.
Để tránh những lo ngại này, một số chuyên gia khuyến nghị rằng nguồn tài trợ nên được hướng đến các mô hình vắc xin đã được thử và thực có nhiều khả năng có thể mở rộng hơn là các mô hình thử nghiệm có thể đòi hỏi hàng tỷ đô la đầu tư cơ cấu trước khi phân phối vắc xin đầu tiên. được sản xuất.
Tuy nhiên, các khoản đầu tư lớn đã được thực hiện trên những thử nghiệm, ngay cả khi chúng đặt ra những thách thức cho việc phân phối đại trà, bao gồm chi phí tiềm năng và yêu cầu nhiệt độ cực lạnh đối với vắc-xin Pfizer-BioNTech cần tủ đông chuyên dụng.
Pfizer và BioNTech dự kiến sản xuất toàn cầu lên đến 50 triệu liều vào năm 2020 và lên đến 1,3 tỷ liều vào cuối năm 2021. Moderna dự kiến sản xuất khoảng 20 triệu liều sẵn sàng xuất xưởng tại Mỹ vào cuối năm Năm 2020 và sản xuất toàn cầu từ 500 triệu đến 1 tỷ liều vào năm 2021.
Tình huống khó xử về đạo đức
Theo dõi nhanh một loại vắc xin giảm thiểu một số kiểm tra và cân bằng được thiết kế để giữ an toàn cho mọi người. Điều này không có nghĩa là làm như vậy là không thể. Nó chỉ đơn giản là đòi hỏi sự giám sát nhiều hơn từ các cơ quan giám sát quản lý như WHO, Viện Y tế Quốc gia (NIH), Cơ quan Thuốc Châu Âu (EMA) và Cục Quản lý Thực phẩm và Dược phẩm Trung Quốc (CFDA), cùng những cơ quan khác, để đảm bảo rằng nghiên cứu được tiến hành một cách an toàn và về mặt đạo đức.
Ngay cả khi có sự giám sát quy định chặt chẽ hơn, cuộc chạy đua sản xuất vắc xin sẵn sàng đưa ra thị trường trong vòng hai năm đã làm dấy lên lo ngại giữa các nhà đạo đức học, những người cho rằng bạn không thể phát triển vắc xin một cách nhanh chóng.vàan toàn.
"Các nghiên cứu thử thách", chẳng hạn, liên quan đến việc tuyển dụng những thanh niên khỏe mạnh, chưa bị nhiễm bệnh trước đó đã tiếp xúc trực tiếp với COVID-19 sau khi tiêm vắc-xin ứng cử viên. Nếu vắc-xin thách thức được chứng minh là an toàn và hiệu quả trong nguy cơ thấp này , bước tiếp theo sẽ là tuyển dụng những người trưởng thành có nguy cơ cao hơn trong một thử nghiệm mù đôi truyền thống. Mặc dù những thử thách như thế này được áp dụng với các bệnh ít gây chết người hơn, như cúm, nhưng việc cố tình để mọi người tiếp xúc với COVID-19 có rủi ro cao hơn đáng kể.
Khi nghiên cứu COVID-19 chuyển từ các nghiên cứu tiền lâm sàng sang các thử nghiệm trên người lớn hơn, những tình huống khó xử như thế này sẽ gây áp lực lên các cơ quan quản lý để quyết định rủi ro nào trong biên giới mới này là "chấp nhận được" và rủi ro nào không.
Bắt đầu từ đâu
Các nhà khoa học không bắt đầu từ đầu khi phát triển các mẫu vắc xin COVID-19 của họ (được gọi là nền tảng). Không chỉ có các loại vắc xin hiệu quả dựa trên các vi rút liên quan mà còn có các loại vắc xin thử nghiệm đã chứng minh khả năng bảo vệ một phần đối với các loại coronavirus như MERS và SARS.
COVID-19 thuộc về một nhóm lớn vi rút được gọi là vi rút RNA bao gồm Ebola, viêm gan C, HIV, cúm, sởi, bệnh dại và một loạt các bệnh truyền nhiễm khác. Chúng được chia nhỏ thành:
- Virus RNA nhóm IV: Chúng bao gồm coronavirus, virus viêm gan, flavivirus (liên quan đến bệnh sốt vàng da và sốt Tây sông Nile), poliovirus và rhinovirus (một trong số những virus cảm lạnh thông thường
- Họ Coronaviridae: Một họ vi rút RNA Nhóm IV bao gồm bốn chủng coronavirus có liên quan đến cảm lạnh thông thường và ba chủng gây bệnh hô hấp nghiêm trọng (MERS, SARS và COVID-19)
Tuy nhiên, cái nhìn sâu sắc về những loại virus này có thể cung cấp cho các nhà nghiên cứu bằng chứng cần thiết để xây dựng và thử nghiệm nền tảng của họ. Ngay cả khi một nền tảng bị lỗi, nó có thể hướng các nhà nghiên cứu theo hướng của những nền tảng khả thi hơn.
Ngay cả trong số nhiều loại vi rút RNA nhóm IV, chỉ có một số ít vắc xin (bại liệt, rubella, viêm gan A, viêm gan B) đã được phát triển kể từ vắc xin sốt vàng đầu tiên vào năm 1937. Cho đến nay, không có vắc xin nào dành cho coronavirus. được chấp thuận và cấp phép đầy đủ tại Hoa Kỳ.
Mô hình phát triển vắc xin
Cuộc chạy đua tìm kiếm vắc xin COVID-19 hiệu quả phần lớn được điều phối bởi WHO và các đối tác toàn cầu như Liên minh Đổi mới Chuẩn bị sẵn sàng Dịch bệnh (CEPI) được thành lập gần đây. Vai trò của các tổ chức này là giám sát bối cảnh nghiên cứu để các nguồn lực có thể được hướng đến những ứng viên có triển vọng nhất.
CEPI đã phác thảo các nền tảng khác nhau có sẵn cho COVID-19 để xây dựng. Một số là các mô hình cập nhật dựa trên vắc xin bại liệt Salk và Sabin của những năm 1950 và 60. Những loại khác là vắc-xin thế hệ tiếp theo dựa trên kỹ thuật di truyền hoặc hệ thống phân phối mới (được gọi là vectơ) để nhắm mục tiêu vào các tế bào hô hấp.
vắc xin protein
Có những lợi ích và hạn chế đối với mỗi nền tảng được đề xuất. Một số loại vắc xin dễ dàng được sản xuất trên quy mô sản xuất nhưng phản ứng của chúng được tổng quát hơn (và do đó, ít có khả năng đạt được tỷ lệ hiệu quả cần thiết để chấm dứt đại dịch). Các mô hình mới hơn khác có thể tạo ra phản ứng mạnh mẽ hơn, nhưng ít người biết về giá vắc xin có thể là bao nhiêu hoặc liệu nó có thể được sản xuất trên quy mô toàn cầu hay không.
Trong số 10 nền tảng vắc xin do CEPI vạch ra, 5 nền tảng chưa bao giờ sản xuất vắc xin khả thi ở người. Mặc dù vậy, một số (như nền tảng vắc-xin DNA) đã tạo ra vắc-xin hiệu quả cho động vật.
Quy trình phát triển vắc xin
Ngay cả khi các giai đoạn phát triển vắc xin được nén lại, quy trình mà vắc xin COVID-19 được phê duyệt sẽ ít nhiều giống nhau. Các giai đoạn có thể được chia nhỏ như sau:
- Giai đoạn tiền lâm sàng
- Phát triển lâm sàng
- Xem xét và phê duyệt theo quy định
- Chế tạo
- Kiểm soát chất lượng
Giai đoạn tiền lâm sàng là giai đoạn mà các nhà nghiên cứu tổng hợp dữ liệu về tính khả thi và an toàn, cùng với bằng chứng từ các nghiên cứu trước đó, để trình các cơ quan quản lý của chính phủ phê duyệt thử nghiệm. Tại Hoa Kỳ, FDA giám sát quá trình này. Các quốc gia hoặc khu vực khác có các cơ quan quản lý riêng của họ.
Phát triển lâm sàng là giai đoạn mà nghiên cứu thực tế được tiến hành ở người. Có bốn giai đoạn:
- Giai đoạn I nhằm mục đích tìm ra liều tốt nhất với ít tác dụng phụ nhất. Vắc xin sẽ được thử nghiệm trong một nhóm nhỏ dưới 100 người tham gia. Khoảng 70% vắc xin vượt qua giai đoạn ban đầu này.
- Giai đoạn II mở rộng thử nghiệm cho vài trăm người tham gia dựa trên liều lượng được coi là an toàn. Phân tích về những người tham gia sẽ phù hợp với nhân khẩu học chung của những người có nguy cơ mắc COVID-19. Khoảng một phần ba các ứng cử viên của Giai đoạn II sẽ lọt vào Giai đoạn III.
- Giai đoạn III bao gồm hàng nghìn người tham gia ở nhiều địa điểm, những người được chọn ngẫu nhiên để tiêm vắc-xin thật hoặc giả dược. Các nghiên cứu này thường bị mù đôi nên cả nhà nghiên cứu và người tham gia đều không biết loại vắc xin nào được sử dụng. Đây là giai đoạn mà hầu hết các vắc xin đều bị lỗi.
- Giai đoạn IV diễn ra sau khi vắc xin đã được phê duyệt và tiếp tục trong vài năm để đánh giá hiệu quả và độ an toàn thực tế của vắc xin. Giai đoạn này còn được gọi là "giám sát sau tiếp thị".
Thuốc chủng ngừa COVID-19: Cập nhật loại vắc-xin nào có sẵn, ai có thể tiêm và mức độ an toàn của chúng.
Thời gian
Nói một cách đơn giản như quy trình này, có một số điều ngoài việc hỏng hóc vắc xin có thể kéo dài thêm vài tháng hoặc nhiều năm cho quy trình. Trong số đó là thời gian. Mặc dù lý tưởng nhất là một ứng cử viên vắc xin nên được kiểm tra trong thời kỳ bùng phát đang bùng phát, nhưng có thể khó biết được vị trí hoặc thời điểm có thể xảy ra.
Ngay cả ở những khu vực bị ảnh hưởng nặng nề như thành phố New York và Vũ Hán, Trung Quốc, nơi dường như sắp bùng phát dịch bệnh hơn nữa, các quan chức y tế công cộng có thể can thiệp để ngăn ngừa dịch bệnh bằng các biện pháp như yêu cầu người dân tự cách ly trở lại. Điều này rất quan trọng để giữ cho mọi người khỏe mạnh, nhưng có thể kéo dài thời gian thử nghiệm vắc xin trong cả mùa hoặc cả năm.
Ứng viên vắc xin trong đường ống
Tính đến tháng 12 năm 2020, 56 ứng cử viên vắc xin được phê duyệt để nghiên cứu lâm sàng, trong khi hơn 165 đang trong giai đoạn tiền lâm sàng chờ phê duyệt theo quy định.
Trong số các nền tảng được phê duyệt để thử nghiệm, vắc xin bất hoạt là một trong những loại vắc xin phổ biến nhất. Điều này bao gồm các tiểu đơn vị protein, sử dụng kháng nguyên (thành phần kích thích tốt nhất hệ thống miễn dịch) thay vì toàn bộ vi-rút và vắc-xin bất hoạt toàn tế bào, một số vắc-xin sử dụng các chất "thúc đẩy" như nhôm để tăng phản ứng kháng thể.
Các vắc-xin RNA và DNA cũng được đại diện tốt, cũng như các vắc-xin vectơ sử dụng vi-rút lạnh bất hoạt để mang các tác nhân vắc-xin trực tiếp đến tế bào.
Các nền tảng bổ sung bao gồm các hạt giống vi rút, vắc xin vectơ kết hợp với các tế bào trình diện kháng nguyên và vắc xin sống giảm độc lực sử dụng dạng COVID-19 sống, được làm yếu để kích thích phản ứng miễn dịch.
(Vương quốc Anh)
(Trung Quốc)
(Hoa Kỳ)
(Hoa Kỳ)
(Hoa Kỳ)
(Trung Quốc)
(Trung Quốc)
(Trung Quốc)
(Hoa Kỳ)
(Trung Quốc)
(Hoa Kỳ)